
1. 雲母とは?
雲母(マイカ、mica)は、薄く剥がれる性質と美しい真珠光沢を持つケイ酸塩鉱物の一種で、層状構造が特徴の「フィロケイ酸塩鉱物」に分類されます。
「フィロ (phyllo)」とは、ギリシャ語で「葉」「薄片」を意味する言葉に由来します。
完全な劈開(へきかい)
劈開とは「割れやすい方向がある」というものですが、その割れ方の容易度によっていくつか区分があります。
劈開が『完全』である場合、「最も簡単に」「きれいな真っ平らに」割ることができます。
雲母を含むフィロケイ酸塩鉱物は、その構造上、薄いシート状に剥離しやすいため、完全な劈開を持っていると言えます。
真珠光沢
真珠の美しい光沢は、真珠が持っている「平らで滑らかな多層構造」から生まれる光の多重反射によって起こる光学効果です。
雲母は、これに似た層状構造と真っ平らな剥離面を持っているので「真珠のような輝き」を示します。
含水鉱物
雲母は、結晶構造のなかに水酸基(–OH)を含む含水鉱物です。
この水酸基は結晶の安定性に寄与し、雲母の構造を特徴付ける重要な要素となっています。
(※一部の雲母は、水酸基(–OH)がフッ素(F)に置き換わっています。)
2. 層状構造
雲母(フィロケイ酸塩鉱物)の最大の特徴は、「層状構造」で、これは、ミルフィーユのように層が幾重にも重なっている構造です。
雲母を構成している層というのは、 TOT層(ティーオーティーそう)と呼ばれるもので、その層と層の間には層間(そうかん)があります。
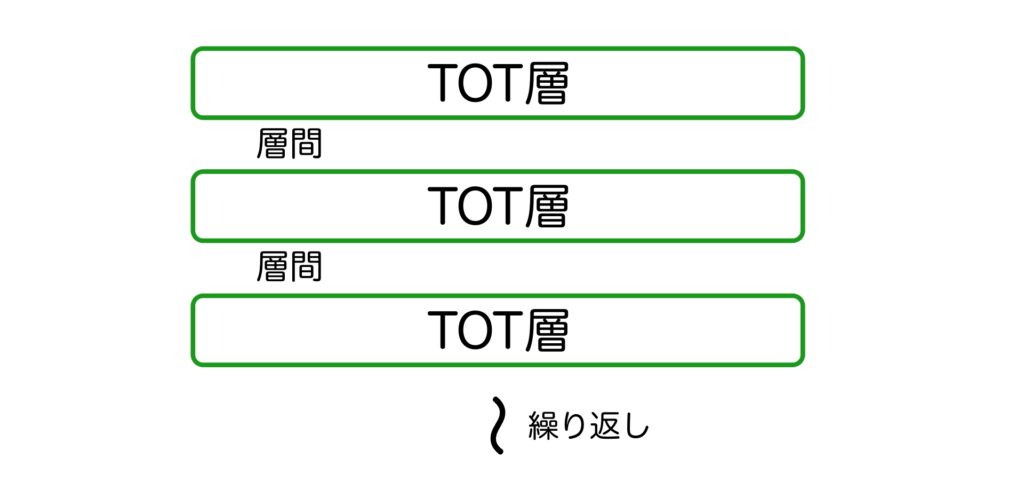
さらに、TOT層の内部はT層とO層から成る3層で構成されています。
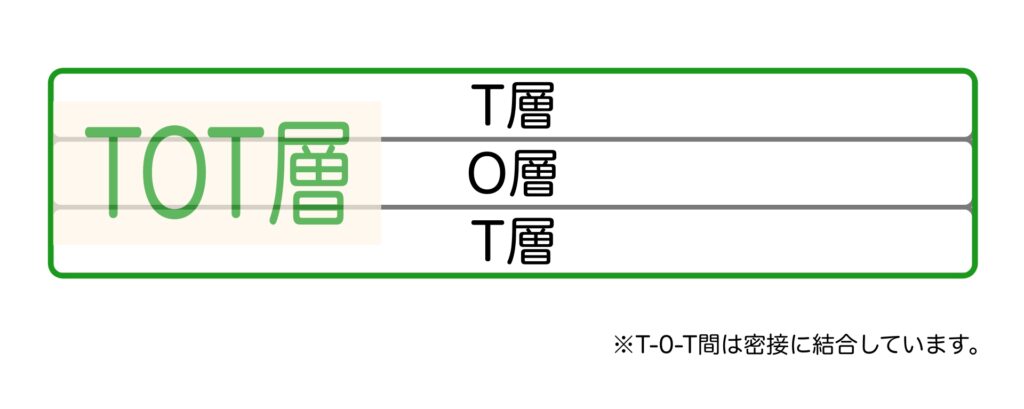
T層:
「Tetrahedral Sheet、テトラヘドラルシート」
意味は ”四面体のシート”
O層:
「Octahedral Sheet、オクタヘドラルシート」
意味は ”八面体のシート”
これは「四面体」や「八面体」の形をした実物が敷き詰められているというものではなく、シートの中にあるのは、あくまで原子という『点』だけです。
その原子の配列において、1つの陽イオンを中心として、その周囲に結合している陰イオンが多面体の頂点に位置するように並んでいる「状態」を指しています。
これを「配位(はいい)」といい、それぞれ「四面体配位」「八面体配位」で構成されているというものです。
以下で詳しくみていきます。
T層(四面体シート)の構造
T層の四面体とは、SiO₄四面体 のことでケイ酸塩鉱物の要の部分です。
そこで、まず前回、前々回のイノケイ酸塩を振り返ってみます。
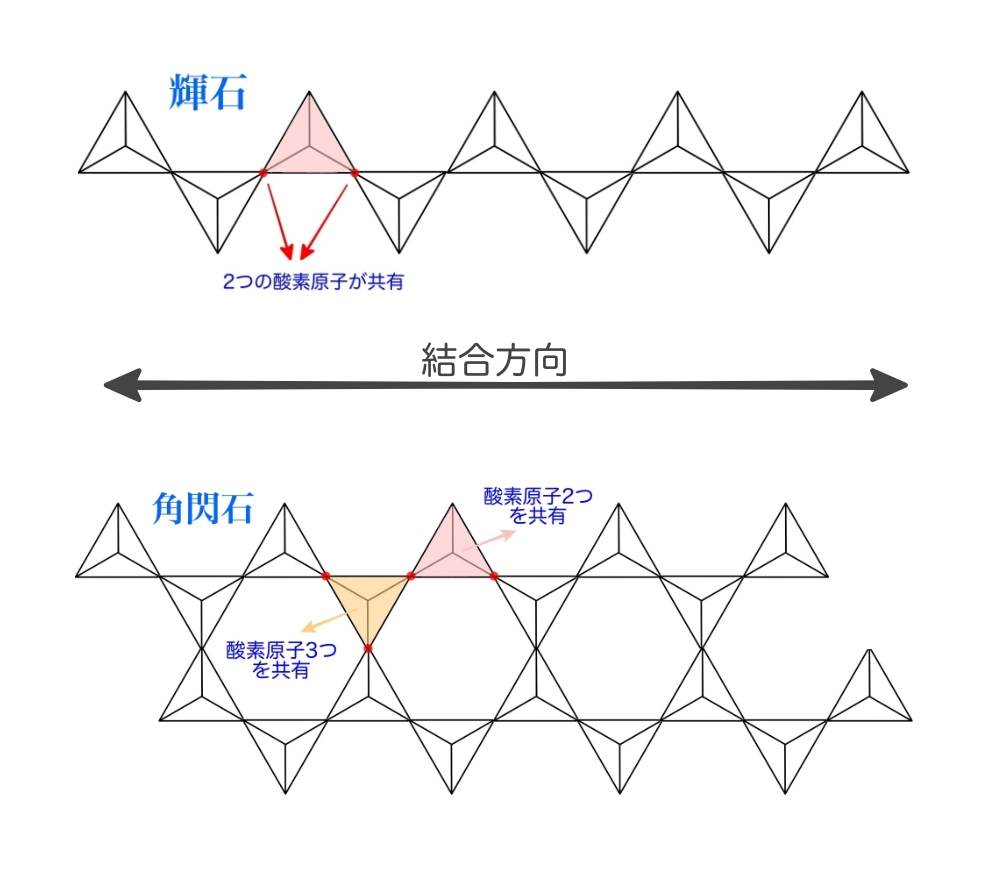
輝石は、SiO₄四面体が持つ4つの酸素原子のうち2つを共有して互いに結びつき、一方向に伸びる鎖を形成していました。
角閃石では、これに加えて鎖と鎖をつなぐ部分でも共有が起こるため、2つを共有する四面体と3つを共有する四面体が交互に並ぶ形で結合しています
この場合も連続する結合方向は、同じく一方向です。
これに対して、雲母(フィロケイ酸塩)の場合は、すべての四面体が酸素原子を3つ共有して互いに結びついているので、結合が二方向(上下・左右)に広がり、2次元のシートを形成します。
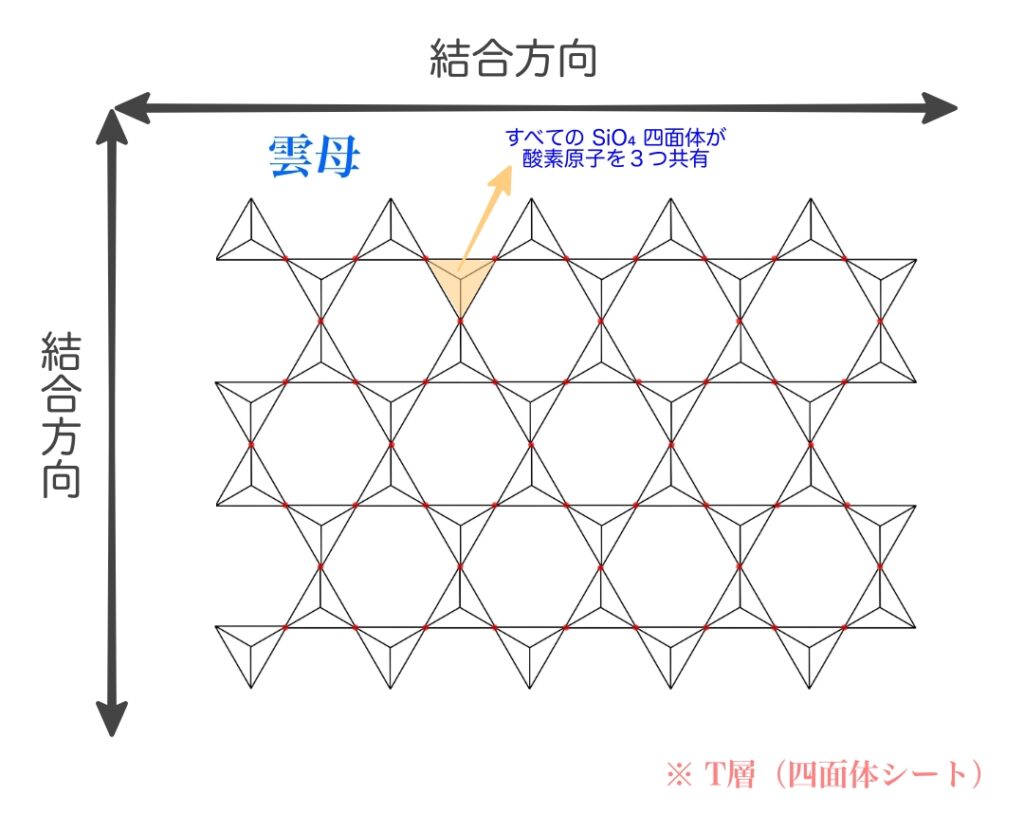
これは、6個の四面体が輪(環)を作っている様子から「六員環(ろくいんかん)ネットワーク」とも呼ばれる構造です。
この平面図を真横から見た断面図は次のようになります。
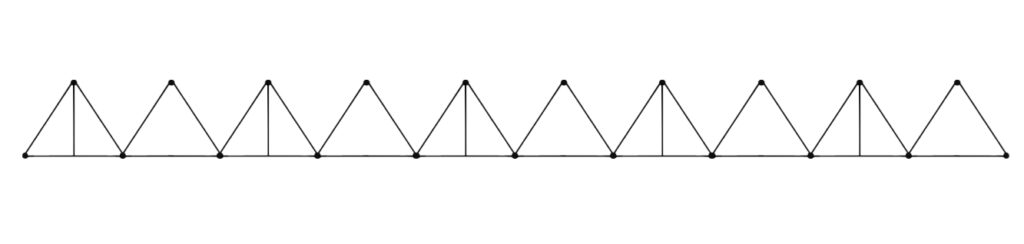
四面体が持つ酸素原子の残りの1つは、このギザギザの頂点部分に位置していて(頂点酸素)、O層の八面体と結合(共有)する役割をします。
O層(八面体シート)の構造
O層の八面体を構成している元素は、金属イオンと酸素イオン(O²⁻)および 水酸基(OH⁻)です。
金属イオンを中心にして O²⁻ と OH⁻ が取り囲むように八面体配位を形成しています。
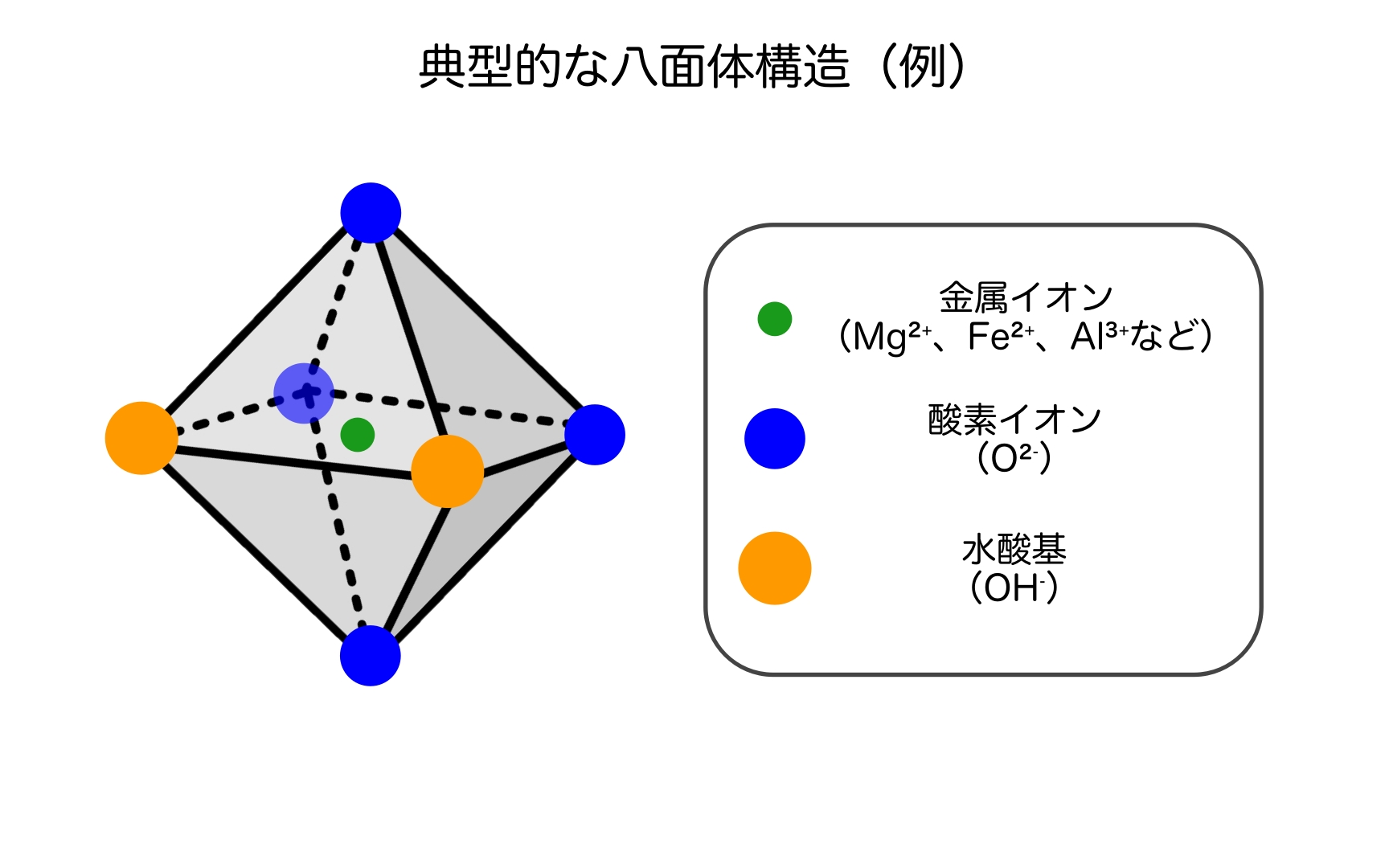
O層は、この八面体が互いに結合し合って平面上に展開したものですが、八面体の向きは上図を少し回転させた角度(酸素原子が上下2つずつになる角度)で並んでいます。
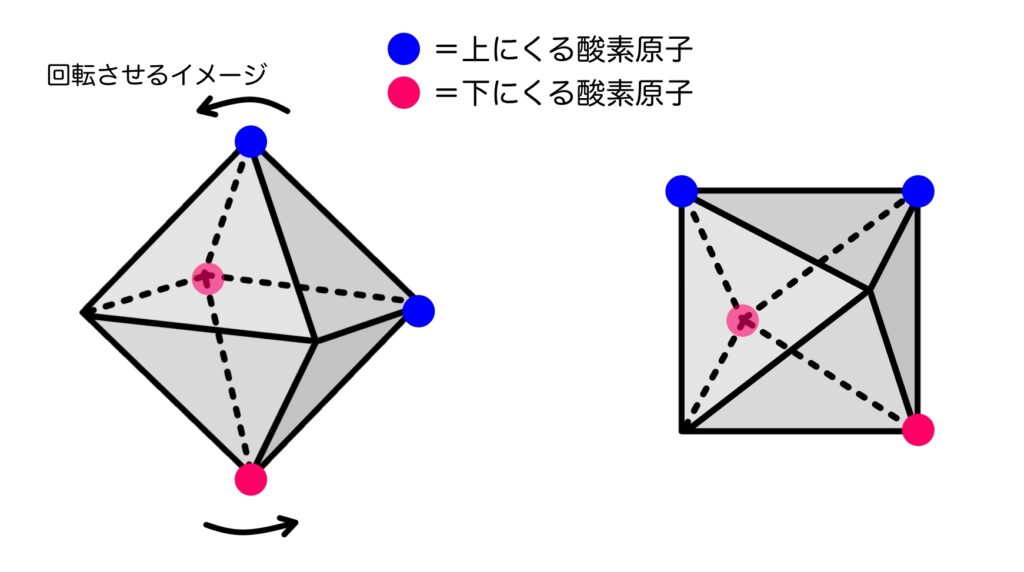
これは、上の酸素原子は上のT層と下の酸素原子は下のT層と結合しているためです。
すなわち、八面体の酸素原子というのはすべてT層の頂点酸素と共有関係にあるのです。
その様子はTOT層のところで示しますので、ここでは具体的な八面体の結合を見ていきます。
隣り合う八面体は、稜(りょう:図形の辺のこと)を共有することで結びついていて、「酸素原子 – 酸素原子」を結ぶ稜と「水酸基 – 水酸基」を結ぶ稜の2パターンあります。
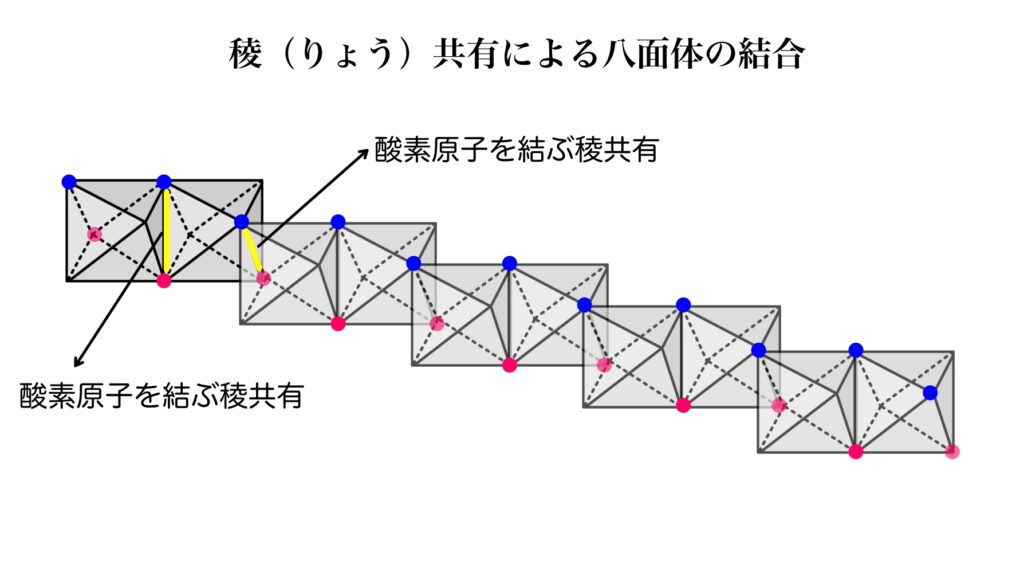
水酸基(図には描いてない)を結ぶ稜は緑色で示した辺です。
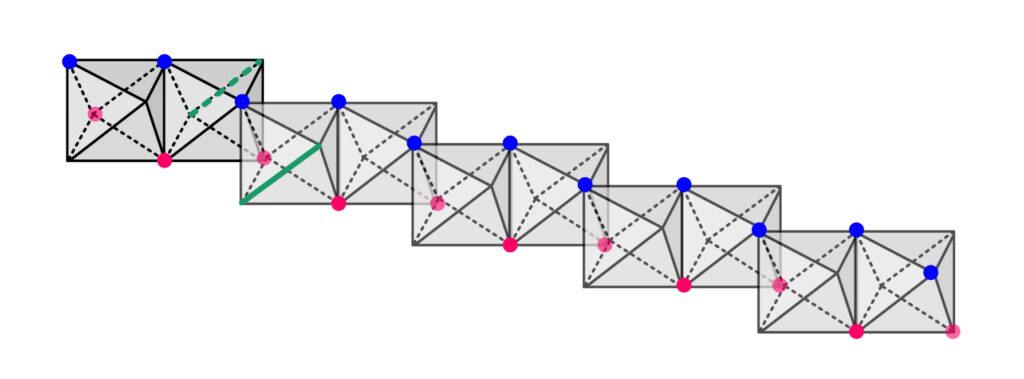
この方向にも結合を展開していくと平面になります。
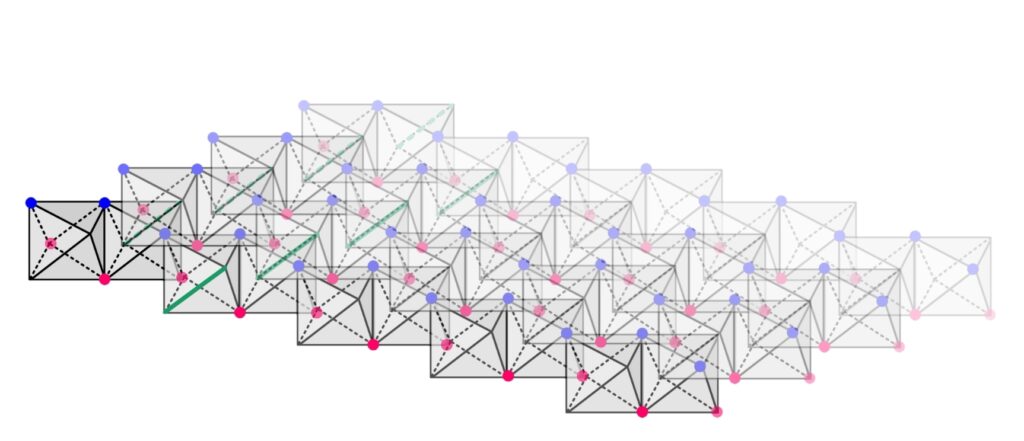
これをさらに真上からみると、蜂の巣状に結合しているのがわかります。
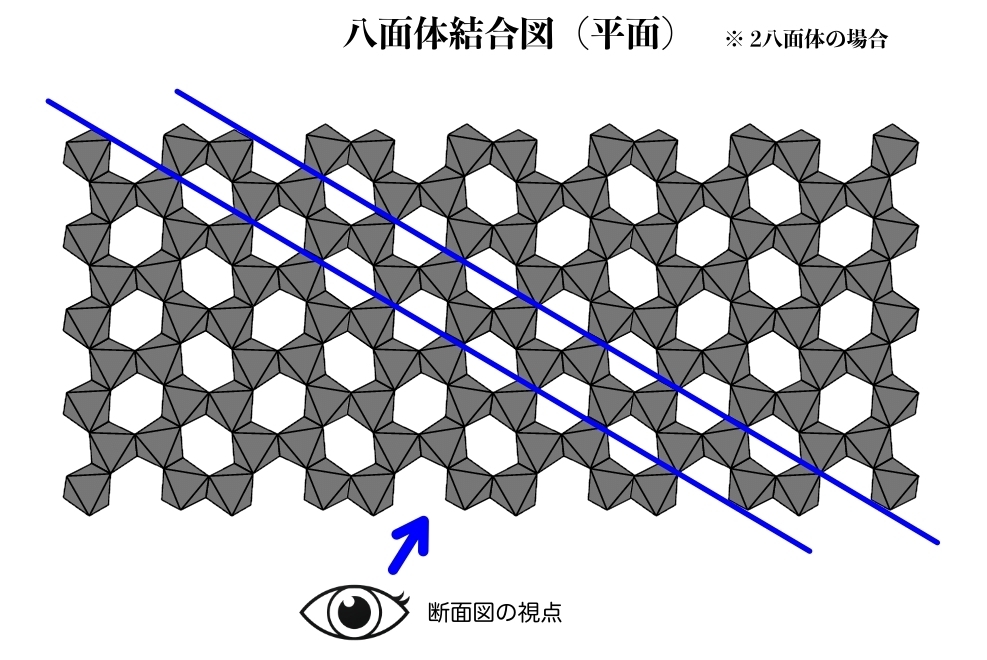
これが雲母の構造のひとつで、結合の合間に空位がある「2八面体」というグループを表しています。
この空位の場所というのは、単にまわりを囲まれてできた空間ではなくて、ちゃんと八面体の骨格(フレーム)を持っている空間です。
つまりここは、八面体配位をとりうる場所で、ただ中心である金属イオンが不在なため”空席” となっているだけなのです。
では、この空席が埋まっている(金属イオンが入っている)とどうなるか?
次のように空位がなくなり、平面が八面体で埋め尽くされます。
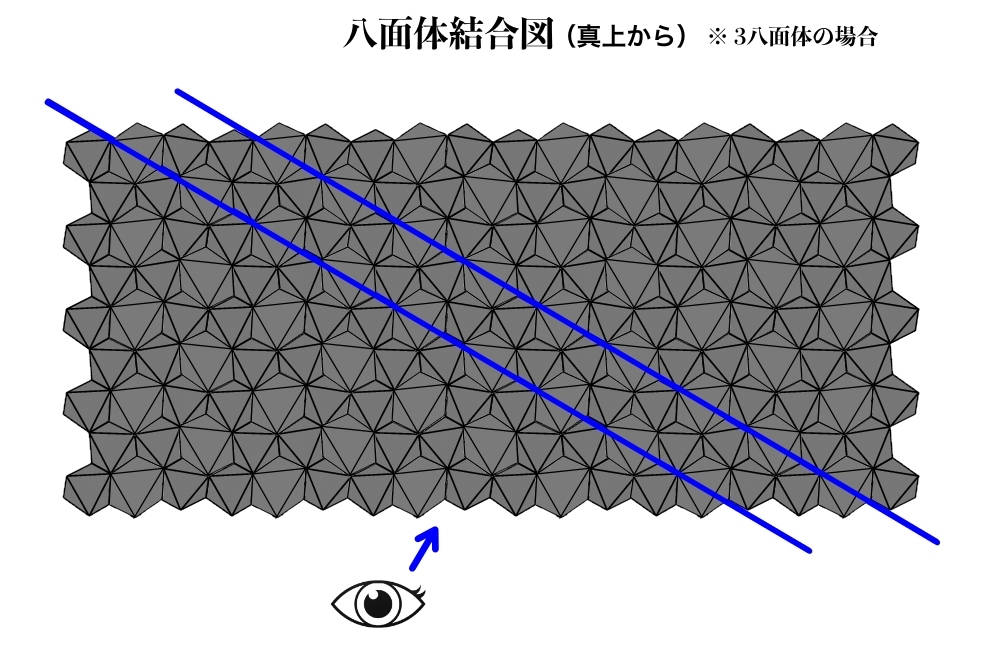
これが、雲母の「3八面体」というグループの構造になります。
断面からからも見てみます。
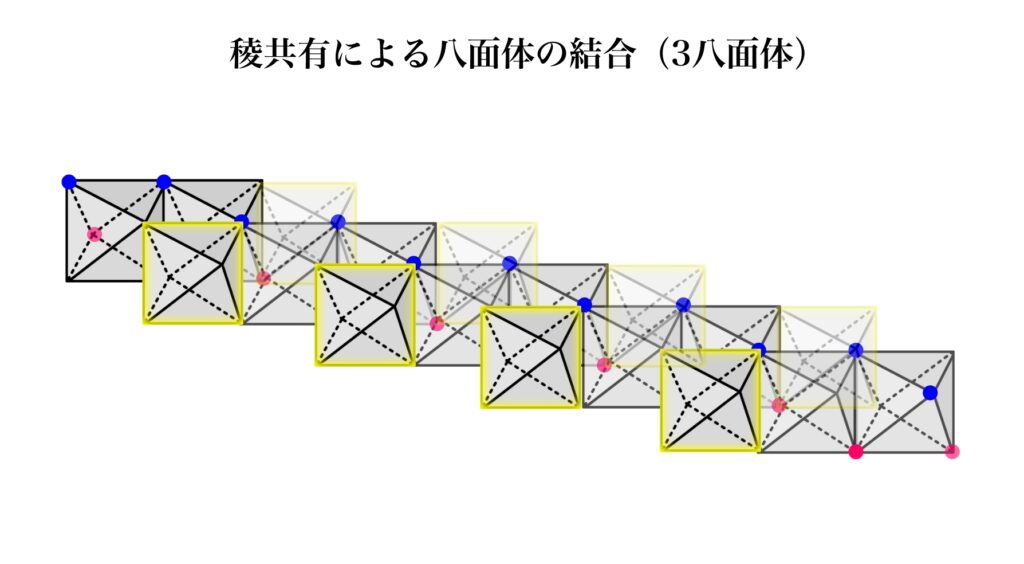
黄色で囲った八面体が、2八面体では空位であった場所です。
つまり、この場所に「金属イオンがあるかないか」が2八面体と3八面体の違いで、構造的な骨格は同じといえます。
(※ただし、空位の存在はエネルギー的なバランスの点から八面体に歪みを生むため、形が完全に同一というわけではありません。)
雲母の分類
雲母の分類は、雲母の最小構成単位(規則的に繰り返される最小のユニット)の基準が、八面体3個であることを起点としています。
1ユニット3個の八面体すべてに金属イオンが入っているものを「3八面体」、2個入って1個が空位となっているものを「2八面体」とし、大きくこの2つのグループに分けています。
TOT層の結合
T層とO層は、酸素原子を介して結合しています。
具体的には、四面体の頂点酸素と八面体の酸素原子が共有関係なっている状態です。
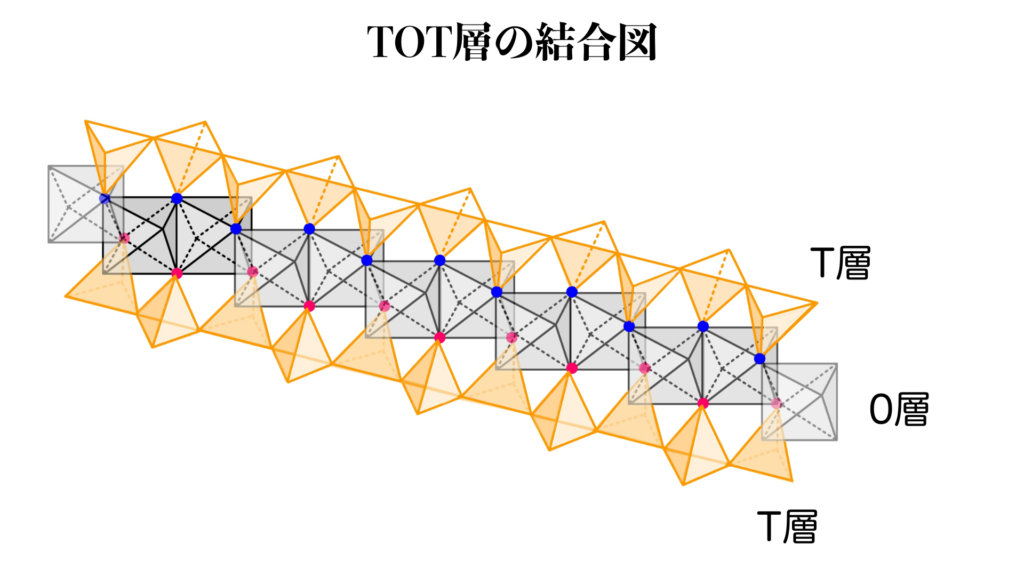
つまり、ここでの酸素原子はT層の四面体の一部であり、O層の八面体の一部でもあるわけです。
シート全体を通してこの共有結合が展開されていて、T層の六員環ネットワークとO層のハニカム(蜂の巣)構造が見事に合わさっています。
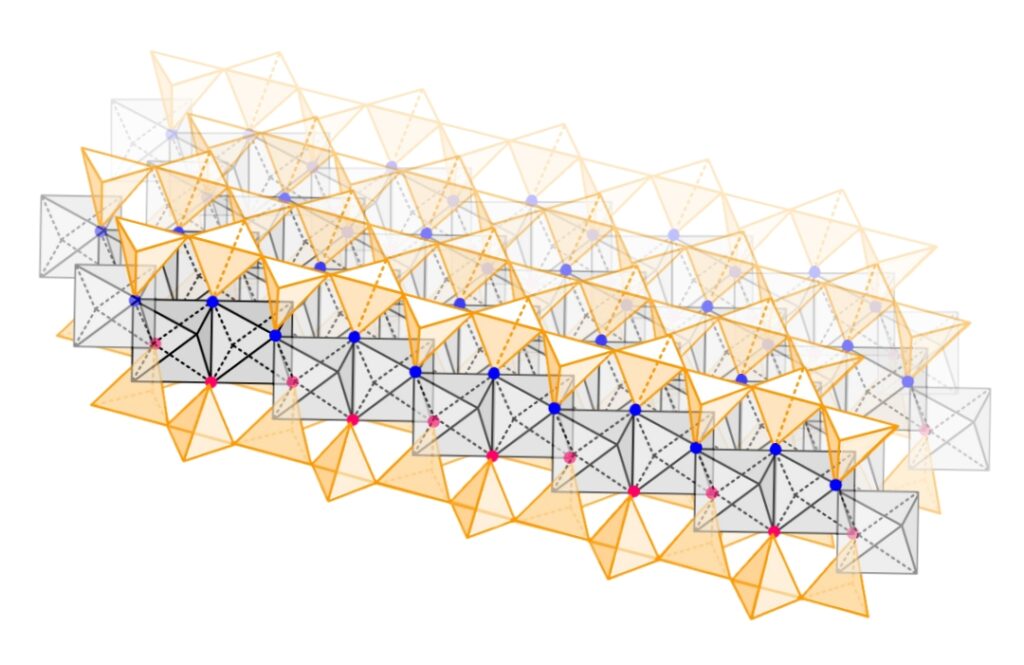
雲母の層間
層状構造はこのTOT層が積み重なったものですが、一般的な雲母では、その層間にはカリウム(K)が入ります。
カリウムはTOT層どうしをつなぐ接着剤の役割を果たしていて、そこには「静電引力(クーロン力)」と呼ばれる、(電気的な中性を保つために)プラスとマイナスが引き合う力が働いています。
この静電引力による結合は、T層 – O層間の共有結合に比べて極めて弱いため、外部から物理的な力が加わった際、強固なTOT層そのものが破壊されるよりも先に、この層間が優先的に剥離します。
これが、雲母の代名詞とも言える『完璧な劈開(へきかい)』を生み出している物理的な正体です。
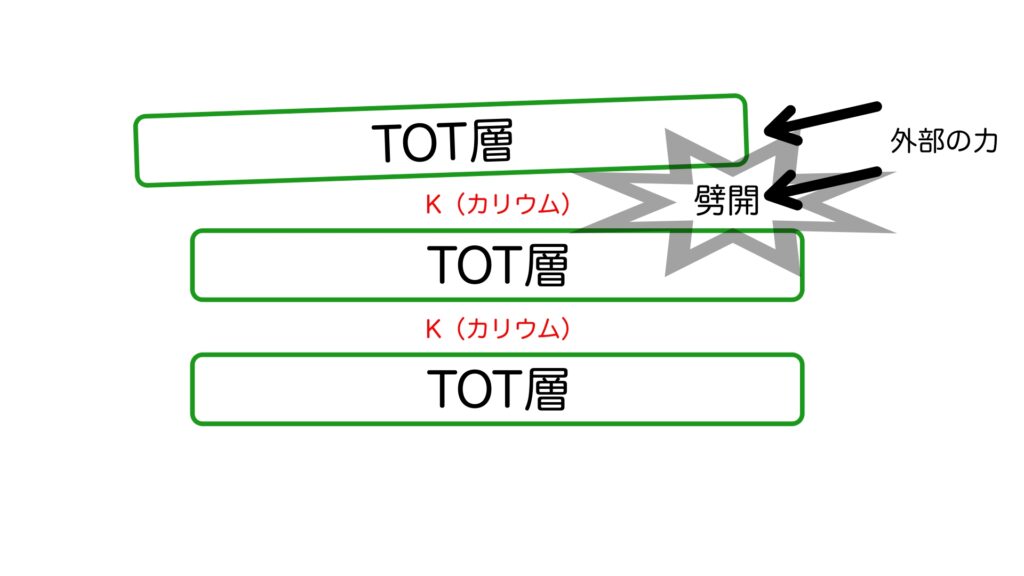
TOT層1枚の厚さは、
およそ1nm(ナノメートル)= 100万分の1mm。
雲母はたしかに「薄く剥がれる」性質を持ってますが、その剥離を人の目で認識できるのは何千何万と積み重なったTOT層の束です。
ここでのポイントは、原子分子レベルで見たときに「雲母の剥離(劈開)は層間で起きている」ということです。
3. 雲母の最小構成単位と化学式
鉱物の化学式は『組成式』とも呼ばれ、鉱物を構成する原子の比率を表しています。
この比率は、鉱物の構造の中で寸分違わず繰り返されるパターンの最小単位、すなわち『最小構成単位』に含まれる原子の数そのものです。
この小さなパターンが何千万回、何億回と積み重なることで、私たちは目に見える大きさの鉱物として観察することができるのです。
雲母の最小構成単位
ここまで見てきた雲母の構造をもとに最小構成単位(1ユニット)を切り出してみます。
TOT層と層間を含んだ最小の単位は次のようになります。
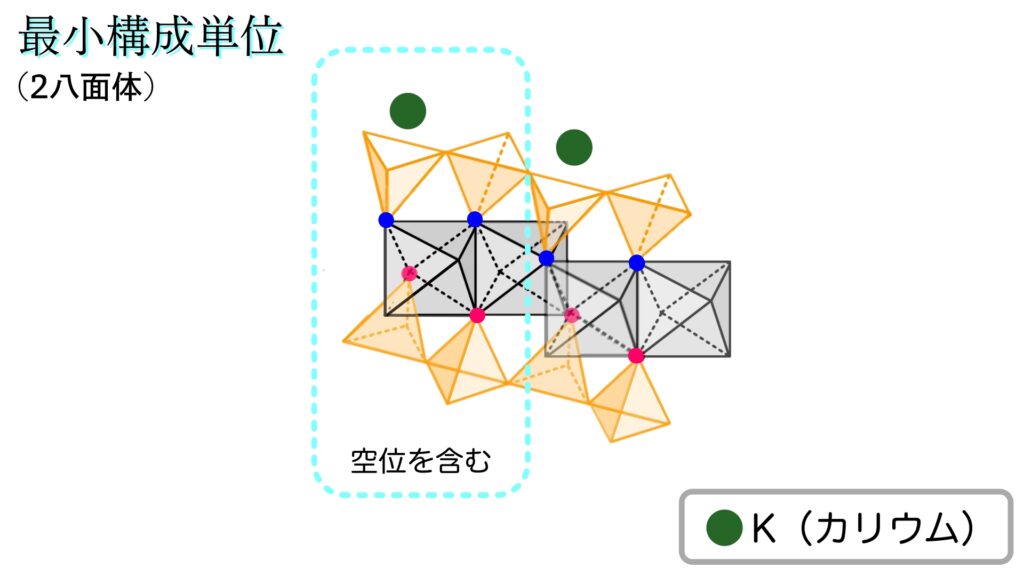
点線で囲った部分が1ユニットに相当します。
最小の基準というのは、前述したようにO層の八面体3個(空位の場合を含めて)です。
そして、この八面体と結合しているのは4個の四面体(上下に2個ずつ)なので、TOT層の最小構成は「四面体4、八面体3」の組み合わせになります。
図は2八面体ですが、3八面体でも同様です。
さらに層間のカリウム(K)を加えると、雲母の最小構成となります。
K + 四面体×4 + 八面体×3
カリウムは1ユニットに1つとなるのですが、その理由は後述します。
では、TOT層の部分(四面体×4 + 八面体×3)にはどんな原子がいくつ含まれているのでしょう?
それにはまず、基本的なTOT層の原子構成から見ていく必要があります。
TOT層内の原子(基本形)
四面体シート内の原子数
「SiO₄四面体」は、その名のとおり Si(ケイ素)1つ と O(酸素)4つから成ります。
単体の四面体が4個であれば ×4 で、
Si₄O₁₆
と単純計算できます。
しかしT層では、四面体の酸素原子はすべて共有関係にあります。
4つのうち3つは隣り合う四面体と、残る1つは頂点酸素として八面体と分け合っています。
なので、半々の1/2で計算しますが、頂点酸素に関しては八面体の分も四面体側でカウントする慣習なので、そのまま1とします。(TOT層で考えれば、結局はO層も足すことになるため)
よって、四面体1個あたりの酸素原子の数は、
1 + 0.5 + 0.5 + 0.5 = 2.5
となり、1ユニット ×4 で 10 となります。
したがってT層の原子数は、
Si₄O₁₀
と表すことができます。
八面体シート内の原子数
単体の八面体では、中心となる金属イオンが1つ、頂点に配位される6つの原子のうち酸素原子が4つ、水酸基が2つが構成原子です。
ここで、酸素原子はすでに四面体側で計上されているので、金属イオンと水酸基について考察していきます。
金属イオンとは、金属元素と呼ばれる原子が電子を放出してプラス(+)の電荷を帯びた状態(陽イオン化)です。
あえて「イオン」と呼んでいるのは、周囲に陰イオン(−)を引きつけるという機能面が重要だからです。
その金属イオンは鉱物種ごとに異なっていて、一様に表すことはできないのですが、中心となり得る原子というのはある程度限られています。
多くの場合、3価のアルミニウム(Al³⁺)、2価のマグネシウム(Mg²⁺)、2価の鉄(Fe²⁺)のうちのどれかが入ります。
最小構成単位における金属イオンの個数は電荷の合計で決まり、通常+6になるように配置されます。
中心に3価の陽イオン(+3)が入った場合、2つまでで2八面体になります。
例:アルミニウム(Al³⁺)
(+3)× 2 = +6
2価の陽イオン(+2)が入った場合は、3つ入って3八面体となります。
例:マグネシウム(Mg²⁺)、鉄(Fe²⁺)
(+2)× 3 = +6
典型例として Al、Mg、Fe に絞って考えると、
(Al₂ or [Mg, Fe]₃)
金属イオンはこのような式で表せます。
これは ”Al が2つ、または Mg か Fe が3つ” という意味です。
続いて水酸基(OH)です。
単体の八面体で2つ配置されているので、1ユニットでは6つと言いたいところですが、ここでもやはり、隣り合う八面体どうしで共有が起きています。
したがって、1ユニットあたりの水酸基の数は実質2つ (OH)₂ になります。
理由は以下の通りです。
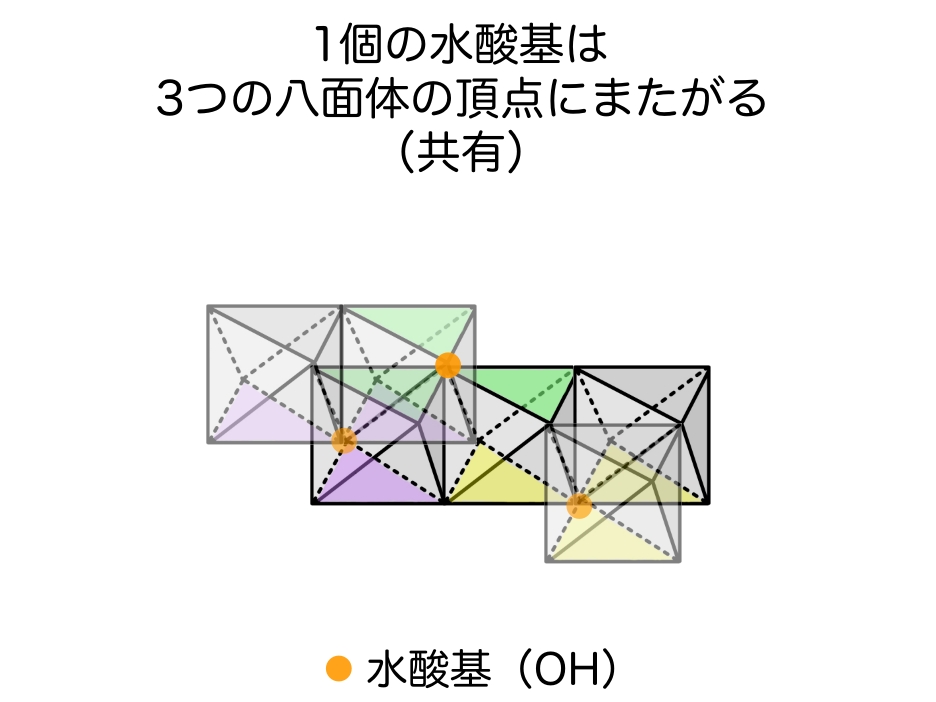
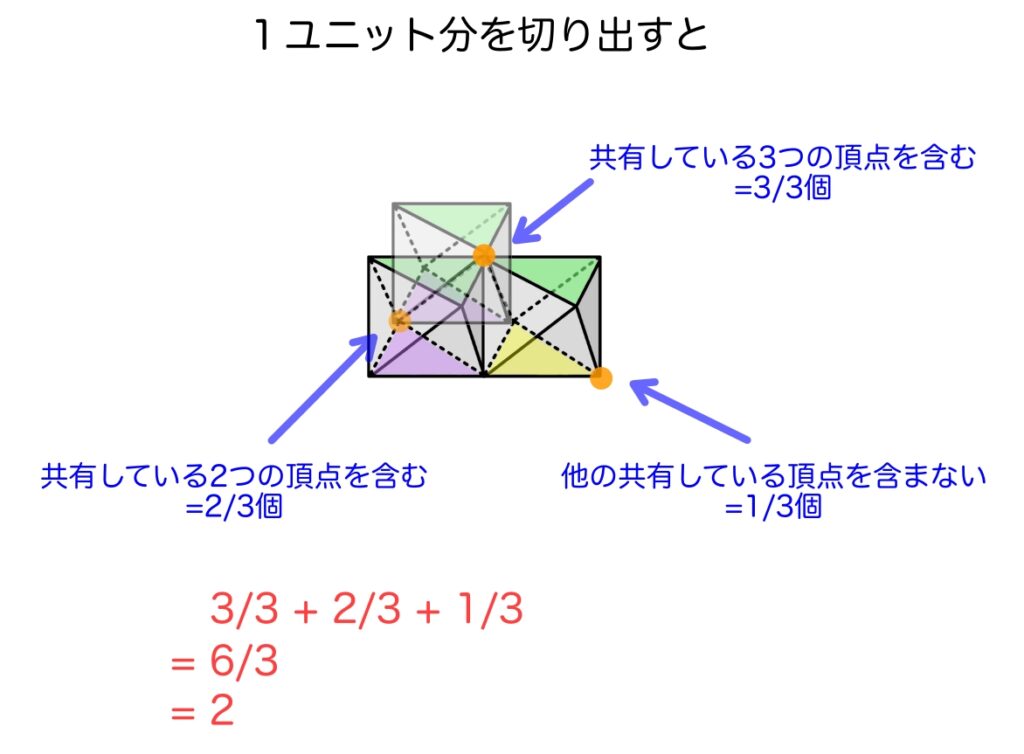
つまり、単体の八面体が持つ2つの水酸基を1ユニットで ×3 しても、共有してる時点で1/3個扱いなので、結局総数は変わらないのです。
金属イオンと水酸基を足したものが、O層の原子数となります。
(Al₂ or [Mg, Fe]₃) + (OH)₂
TOT層全体の原子数
T層:Si₄O₁₀
O層:(Al₂ or [Mg, Fe]₃) + (OH)₂
それぞれの層の原子数がわかったところで、これらを合わせてTOT層の原子数としてまとめます。
これは、そのまま(典型的な)TOT層を表す化学式になります。
(Al₂ or [Mg, Fe]₃)Si₄O₁₀(OH)₂
TOT層の骨格となる部分は Si₄O₁₀(OH)₂ です。
(Al₂ or [Mg, Fe]₃) の位置にくる原子は、典型例以外の金属イオンである場合も含めて変数となる部分です。
基本形のままのTOT層を持った鉱物で知られているのが、タルク(滑石:かっせき)です。
このタイプのフィロケイ酸塩は、TOT層だけで形成されている(層間が無い)という大きな特徴を持ちます。
化学式:Mg₃Si₄O₁₀(OH)₂
いたってシンプルな化学式で、八面体の中心はマグネシウム(Mg)で3八面体型であることがわかります。
層間を持たないということはTOT層が直に結合している構造をとるため、その結びつきはファンデルワールス力という非常に弱い力に限定されます。
これは、雲母の層間に働く静電引力(クーロン力)よりも極めて微弱な力です。
そのゆえ、ある程度の厚みをもった「層の束」として剥がれるのではなく、原子分子レベルで1枚1枚のTOT層が ”滑る” ようにズレて剥離します。
厚みを維持できないので粉末状にもなりやすく、爪で引っかくだけで容易に白い粉(微細な結晶の破片)へと分解されます。
粉末化したタルクの粒子は「さらさら・すべすべ」とした感触が特徴的なのですが、これもミクロな層の滑りによるものです。
その剥離のしやすさゆえに、タルクはモース硬度の基準になっています。
モース高度:1
雲母のTOT層
タルクに層間が無いのは、TOT層が本来の形を保っているためです。
それは ”TOT層内で電荷のバランスが取れている状態” であり、その意味では理想的なTOT層とも言えますが、そこで完結してしまっているがゆえに、それ以上の結合の広がりが生まれずに ”ただTOT層が積み重なっているだけ” と捉えることもできます。
では、雲母の場合はどうでしょう?
Al置換
雲母のTOT層は、その内部でAl置換が起きているという特徴を持っています。
Al置換とは、SiO₄四面体の中心である Si(ケイ素)が Al(アルミニウム)に置き換わった状態をいいます。
四面体:SiO₄ → AlO₄
一般的な雲母の場合、1ユニット内の四面体4個のうち1個が Alに置き換わっています。
T層:Si₄O₁₀ → AlSi₃O₁₀
したがって、雲母のTOT層は、
(Al₂ or [Mg, Fe]₃)AlSi₃O₁₀(OH)₂
このような式になります。
層の基本構造は全く同じです。
層間の役割
Al置換がTOT層にもたらす影響は電荷バランスです。
Si というのは、陽イオンで4価の電荷(Si⁴⁺)を持っています。
それが3価の Al³⁺ に置き換わるということはそのぶん電荷の不足が発生し、TOT層全体としてマイナスの電荷を帯びます。
ユニット内で見ると、置換が1個であればマイナス1の電荷を持つことになり、これを補うためにTOT層外に追加のイオンが引き寄せられます。
これが層間にあたるカリウム(K)です。
カリウムは1価の陽イオン(K⁺)なので、ちょうど1個入ることで電荷が安定します。
雲母の最小構成のところで触れた、1ユニットにカリウムが1個である理由です。
層間は、バランスが崩れたTOT層の電荷を中和するだけでなく、引き寄せられたイオンとの間に働く静電引力(クーロン力)によって層の結合を強化する役割をしています。
雲母の化学式
雲母の最小構成の解像度を上げていくと
TOT層と層間の1ユニット
⬇︎
K + 四面体×4 + 八面体×3
⬇︎
K(Al₂ or [Mg, Fe]₃)AlSi₃O₁₀(OH)₂
最終的には化学式にたどり着きます。
この式はあくまで典型的な雲母を表したものではありますが、これを理解することで、その他の雲母あるいはフィロケイ酸塩についても、どこが違うのか、何が異なるのかが把握しやすくなります。
4. 脆雲母
雲母の典型との相違点には、以下のようなケースがあります。
その他の雲母の主なケース
- 層間がカリウム(K)ではない
- 八面体の中心が Al、Mg、Fe 以外
- 1ユニット内でAl置換が2個起きている
- 水酸基(OH)がフッ素(F)に置き換わっている
これらは単独というよりも因果関係で複合的に発生します。
最後に、その一例として脆雲母(ぜいうんも)を取り上げます。
脆雲母(ぜいうんも)
”1ユニット内に2個のAl置換” が起きた場合、電荷不足は −2 になるため、1価のカリウムでは補いきれなくなります。
そこで、カリウムに代わり ”層間に2価の陽イオン” が入ることで、電荷バランスを維持している雲母を「脆雲母(ぜいうんも)」と呼びます。
広義には雲母の仲間ですが、性質が異なる別グループの雲母です。
明確に区別する意味で、一般的な雲母のグループを「純雲母(じゅんうんも)」と呼ぶこともあります。
脆雲母の脆(ぜい)は、脆い(もろい)という意味ですが、層間がカリウムである場合と比べると2価の陽イオンが入ったほうが層間の結合は強くなります。(静電引力は増大する)
ただ、層間の強度が増すということは、剥離して外部からの力を層間で逃がすことができなくなり、TOT層そのものが壊れやすくなります。
その意味で「脆い」というわけです。
ゆえに、脆雲母は”薄く剥がれる” という一般的な雲母の性質(完全な劈開)を持っていません。
脆雲母の代表的なものには、真珠雲母(しんじゅうんも:マーガライト)があります。
化学式:CaAl₂(Al₂Si₂)O₁₀(OH)₂
2個のAl置換:(Al₂Si₂)O₁₀(OH)₂ を持ち、層間に2価のカルシウムイオン(Ca²⁺)が入っています。
八面体の中心にもアルミニウム:Al₂(※Al置換ではない)を持つ2八面体型です。
名前の由来は「真珠光沢」ですが、真珠光沢自体は雲母全般に共通する特徴とも言えます。
それが純雲母ではなく、脆雲母の鉱物種に名付けられてるのは、皮肉にも脆雲母のほうがより真珠に近い「しっとりした」輝きを示しているからです。
これは ”脆さ” から生まれる「層内部のミクロな無数のひび割れ」が、より光を散乱(内部反射)させるため、輝きに「深み」を与えていると考えられています。
5. 後編につづく
かなり長文になってしまったので、前後編に分けることにします。
後編では、具体的な雲母の種類について見ていきます。
産出量の多い代表種のほか、少し複雑な構造を持つレピドライトや変種であるフックサイトといった市場でよく目にするものについても考察します。
また、インクルージョンという形で雲母を内包しているもの(マイカインクォーツなど)も取り上げます。


