
「ダイヤモンド」とは
【ダイヤモンド】
和名 : 金剛石(こんごうせき)
組成式 : C(炭素)
結晶系 : 立方晶系(等軸晶系とも言う)
主な特徴
- 炭素(C)のみから成り立っている。
- モース硬度は最高の10
- 屈折率(くっせつりつ)が非常に高い

ざっくり言うと、屈折率が高いほど輝きが生まれます。
ダイヤモンドの形成過程
1. 形成の環境:
ダイヤモンドは、地球のマントル内、深さ約150km以上の地点で、高温・高圧の条件下で形成されます。
この環境下においては、炭素はダイヤモンドの結晶構造を取ることが熱力学的に有利(安定な状態)となります。

マントルは、地球の表面である地殻のさらに下です。

1200℃以上の温度と大気の5万倍の圧力といわれます。
このような条件下では、物質はエネルギーをできるだけ低くして、より安定な状態を求める傾向があります。
なので、炭素原子はできるだけ互いに近づき、最もコンパクトにまとまろうとします。
このコンパクトな構造が、ダイヤモンドの結晶構造です。
ダイヤモンドが硬い理由
▷炭素原子の性質
炭素原子は4つの原子と結びつくことができますが、
その4つ全てが、炭素原子同士の結びつきによる「炭素 – 炭素の共有結合」をしています。

この炭素原子間の共有結合は非常に強固です。

SiO₂(石英)も共有結合を持ちますが、炭素-炭素の結合の強度は、
「Si(ケイ素)- O(酸素)」の結合よりも強いです。
それは、炭素は小さい原子であり、他の炭素原子と非常に近接して結合できるためで、
その結果、結合は強く、短くなります。
▷密な四面体構造
各炭素原子は、他の4つの炭素原子と四面体構造を形成して結合しています。

この四面体構造では、各炭素原子が空間的に均等に分布し、極めて均一で対称的な構造になります。
これにより全方向に等しく力が分散されるため、特定の方向に弱点が存在しない強固さをもたらします。
▷結晶の連続性
ダイヤモンドの結晶は、中断や不純物の少ない、連続した炭素のネットワークで構成されています。
この一貫した結晶構造が、外部の力に対する強い抵抗力を持つ理由となります。
これらの要因が重なって、
ダイヤモンドの非常に硬く、そしてエネルギー的にも安定した構造が生まれます。

また、これらは高い屈折率をもたらす要因にもなっています。
2. 地表への運搬:
ダイヤモンドが形成された後、地下深部から急速に地表へと運ばれる過程が必要です。
この役割を果たすのがキンバーライトというマグマです。
キンバーライトは、マントルの深部から急速に上昇し、その際にダイヤモンドを含むマントルの断片を引き上げます。

現在あるダイヤモンドの鉱床(未発見のものを含む)は、
はるか昔の地質的活動や火山活動によってできたものです。
ここで重要なのが、
『急激に上昇する』ということです。
マグマの上昇がゆっくりであれば、ダイヤモンドはグラファイトに変わってしまう可能性があります。

グラファイト?
【グラファイト】
和名 : 石墨(せきぼく) ※または黒鉛
組成式 : C(炭素)
結晶系 : 六方晶系

鉛筆の芯に使われる黒っぽい物質です。

昔はグラファイトに鉛(なまり)が含まれていると考えられていたので
”黒鉛(こくえん)” とも呼ばれています。
ダイヤモンドとグラファイトはどちらも炭素の結晶ですが、異なる結晶構造(結晶系)を持ちます。
ゆえに、見た目も硬さも全く違います。
ダイヤモンドは三次元的な四面体構造で結合していますが、
グラファイトは二次元の平面上で六角形のリング構造を形成しています。
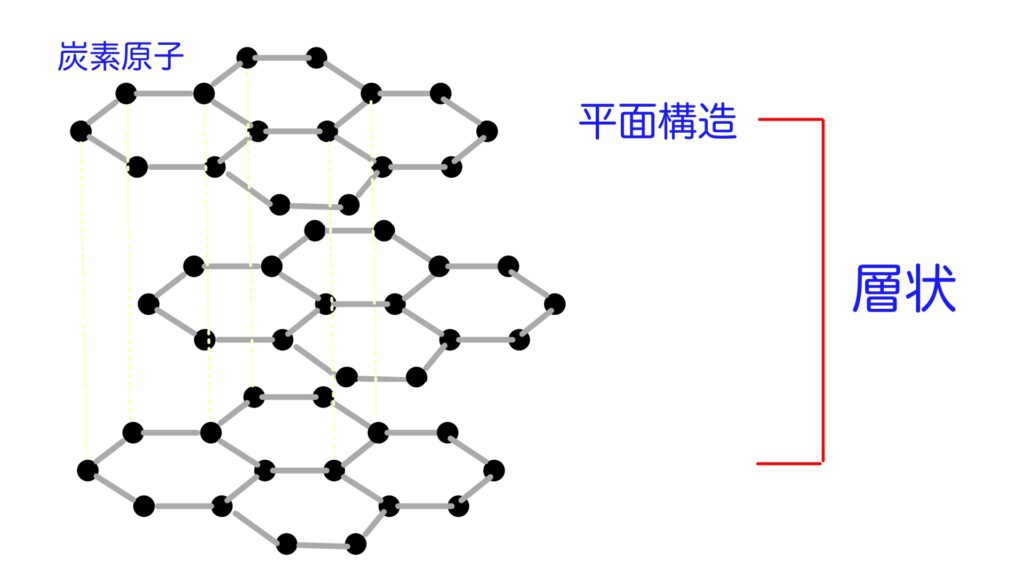
そして、これらが層状に重なって結合しています。
各層は非常に弱い結合であるため、層と層との間は滑りやすい特性があります。

ミルフィーユ状態です。

紙に押しつけた摩擦力で容易にはがれるため、鉛筆で文字が書けるわけです。
話を戻すと、
ダイヤモンドがグラファイト化してしまう原因は、炭素原子の安定性にあります。
地表に近い低温・低圧の環境下では、
炭素原子はダイヤモンドの形態であるより、グラファイトであるほうが安定的である。
キンバーライトがゆっくりと上昇すると、ダイヤモンドが低温・低圧の環境にさらされる時間が長くなります。
この結果、ダイヤモンドはより安定なグラファイトに変わってしまう可能性が高まります。

炭素原子の再配列 =『再結晶』が起こります。

なので変化が起きる前に、
地表近くまで運ばれることが必要なのです。
3. 冷却と固化:
キンバーライトが地表近くまで到達すると、急速に冷却・固化します。
この過程で、ダイヤモンドを含むキンバーライト岩(キンバーライトパイプ)が形成されます。

冷え固まったキンバーライトは ”ダイヤモンドの母岩” となります。

また、マグマが通った「通り道」にも筒状の鉱床を形成します。

結晶化について
石英の結晶化に代表されるように、
ケイ酸塩鉱物は通常、溶けた液体がゆっくり冷え固まって結晶化します。
したがって、鉱物全体で見ても冷却による結晶がほとんどになります。
しかし、ダイヤモンドの形成に見られるように高温・高圧の条件下で結晶化する鉱物もあります。

『ペリドット』がそうです。

ペリドットについては、いずれまた詳しく見ていきます。
たぶん。。。
また、『凝華(ぎょうか)による結晶化』というものもあります。
物質が気体の状態から直接固体の状態に変わる現象を指します。
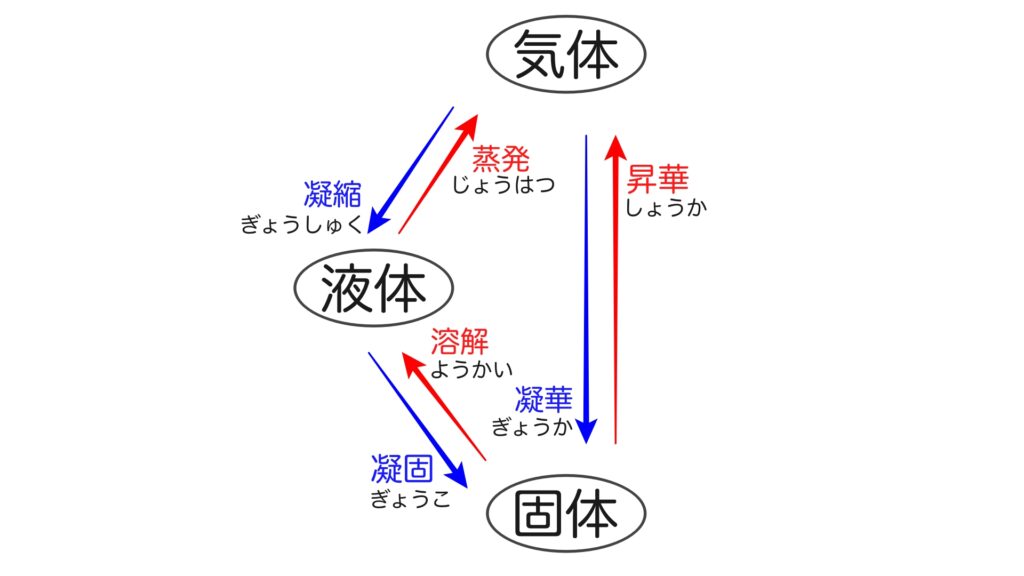
大気中の水蒸気が ”雪の結晶” に変わる過程は、この凝華による結晶化です。


ん?ということは、もしかして…

そうです。”雪の結晶” は「鉱物」です。
そして、水が凝固してできる『氷』もまた、
「自然界で形成され、無機の固体であり、特定の化学組成と結晶構造を持っている」ため、
定義上、鉱物に分類されます。

雪の結晶は氷の一形態として扱われます。
【氷または雪の結晶】
組成式 : H₂O
結晶系 : 六方晶系

この場合の「氷」は自然界にできる氷のことです。
冷蔵庫の中や実験室での氷は当てはまりません。

ちなみに説明は省略しますが、
『霜(しも)』や『雹(ひょう)』も同様と考えてください。



