
1. 地球の表面を形成する鉱物
”ケイ酸塩鉱物” という言葉は、天然石の本などで、必ずと言っていいほど出てくる用語です。
その理由は、ケイ酸塩鉱物が地球の表面(地殻【ちかく】)を形成する鉱物の約90%を占めているためで、いわば、ほとんどの鉱物がケイ酸塩鉱物と言えるからです。
その内訳を鉱物種別に見ると、下の図のようになります。
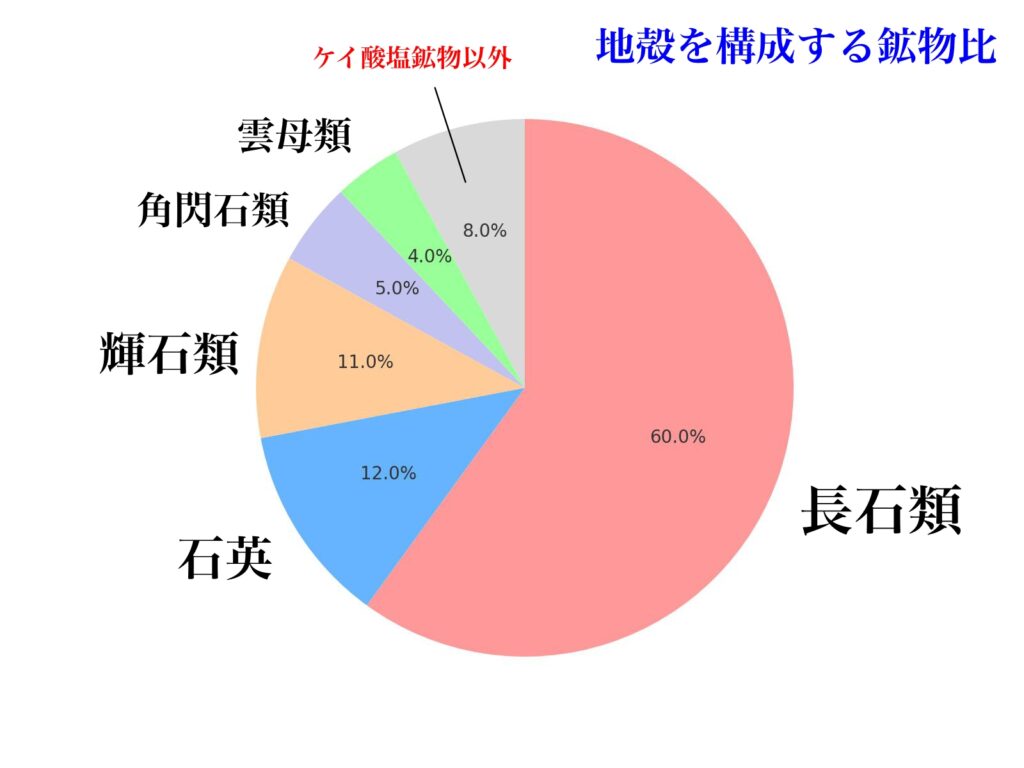
※おおよその割合です。
- 長石(ちょうせき)類:フェルドスパー
地殻の約60%を占め、最も豊富なケイ酸塩鉱物です。
サンストーン、ムーンストーン、ラブラドライト、アンデシン、アマゾナイトなど。 - 石英(せきえい):クォーツ
約12%を占めます。
水晶、カルセドニー、アゲート、ジャスパーなど。 - 輝石(きせき)類:パイロキシン
約11%を占めます。
翡翠、クンツァイト、ハイパーシーン、ブロンザイトなど。 - 角閃石(かくせんせき)類:アンフィボール
約5%を占めます。
ネフライト、ヌーマイトなど。 - 雲母(うんも)類:マイカ
約4%を占めます。
モスコバイト、フックサイト、レピドライトなど。 - その他のケイ酸塩鉱物
総じて1%に満たないので、構成比には含まれていません。
ガーネット、トルマリン、オリビン(ペリドット)、スピネルなど。
ここまでがケイ酸塩鉱物です。
【参考】
ケイ酸塩鉱物以外の鉱物は、全体の約8〜10%程度です。
まとめて「非ケイ酸塩鉱物」として分類されますが、参考までに代表的なものをいくつか挙げます。
- 炭酸塩鉱物
(たんさんえんこうぶつ):
炭酸(CO₃)イオンを含む鉱物。
カルサイト(CaCO₃)
ロードクロサイト(MnCO₃)
マラカイト(CuCO₃)
など。 - 硫酸塩鉱物
(りゅうさんえんこうぶつ):
硫酸(SO₄)イオンを含む鉱物。
石膏(CaSO₄·2H₂O)
天青石(SrSO₄)
など。 - リン酸塩鉱物
(リンさんえんこうぶつ):
リン酸(PO₄)イオンを含む鉱物。
アパタイト(Ca₅(PO₄)₃(F,Cl,OH))
ターコイズ(CuAl₆(PO₄)₄(OH)₈·4H₂O)
など。 - ハロゲン化鉱物
(ハロゲンかこうぶつ):
ハロゲン元素(塩素、フッ素、臭素、ヨウ素)を含む鉱物。
岩塩(NaCl)
フローライト(CaF₂)
など。 - 酸化鉱物
(さんかこうぶつ):
酸素と金属元素の化合物からなる鉱物。
コランダム(Al₂O₃)
ヘマタイト(Fe₂O₃)
ルチル(TiO₂)
など。 - 硫化鉱物
(りゅうかこうぶつ):
硫黄と金属元素の化合物からなる鉱物。
黄鉄鉱(FeS₂)
など。
2. ケイ酸塩とは?
ところで、ケイ酸塩鉱物とはどんな鉱物なのでしょうか?
「ケイ酸塩」の意味とは?
ケイ酸塩の ”ケイ酸” は、
『ケイ素(Si)と酸素(O)からなる化合物』
を意味します。
※ただの「ケイ酸」は、水溶液の状態です。
わかりやすい具体例は、 石英(水晶)の主成分である『二酸化ケイ素:SiO₂』です。
では、”塩” は?
塩は、化学用語の ”えん” と呼ばれる化合物の総称です。
陽イオン(プラスの電荷を持つ)と陰イオン(マイナスの電荷を持つ)が結合して電気的に中性になった化合物
ですが、ここではとりあえず、
電気的なバランスを取るために「何か」とくっついた
と考えてください。
まとめると、
「石英の成分」と「何か」が結合して「電気的に中和された」化合物
が ”ケイ酸塩” のイメージです。
そして「ケイ酸塩鉱物」は、このケイ酸塩でできています。
地殻の大部分を網羅するほど、その種類は豊富ですが、なぜそんなに種類が多いのでしょう?
その理由を探るため、次でケイ酸塩を化学的にもう少し深く見ていきます。
「ケイ酸塩」と「ケイ酸塩鉱物」はつながりが深いので、結局のところ、言葉の説明としては同じ内容に行き着きます。
なので、「ケイ酸塩」といえば「ケイ酸塩鉱物」のことだと考えて良いです。
3. ケイ酸塩の構造
ケイ酸塩のもととなるのは『ケイ素(Si)と酸素(O)から成る化合物』つまり『石英の成分』と言いましたが、
正確には、
ケイ酸イオン(SiO₄⁴⁻)
と表現されます。
そして重要なのが、その構造です。
ケイ素原子1つと酸素原子4つが結合した四面体構造をしていて、
SiO₄四面体(エスアイオーフォーしめんたい)
と呼ばれます。
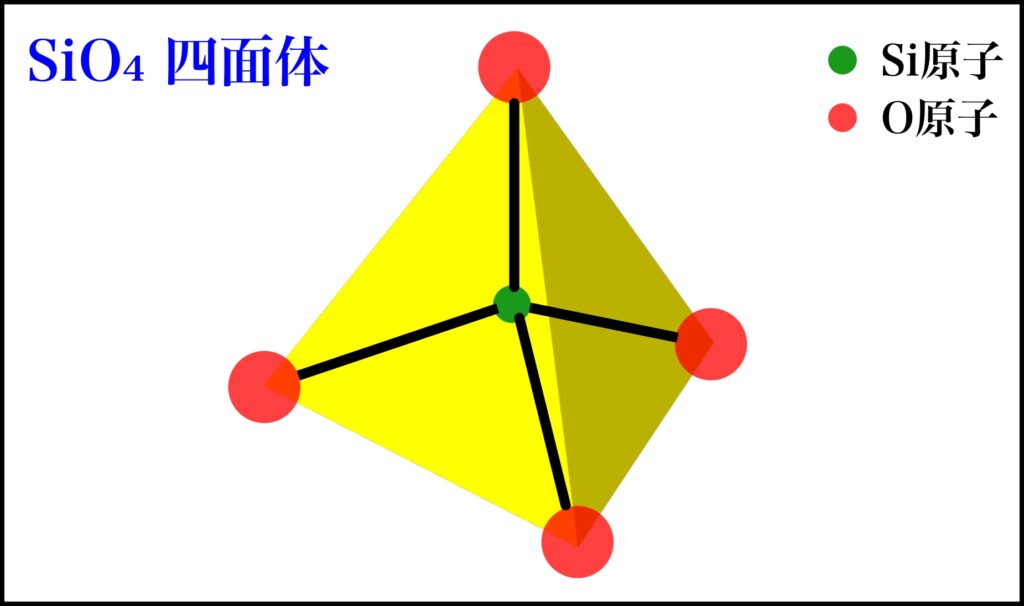
※すべてのケイ酸塩鉱物の基本構造です。
では、なぜイオン(SiO₄⁴⁻)なのか?
SiO₄四面体の電荷
イオンとは、原子が電気を帯びた状態を指します。
正(プラス)の電気を帯びたものを陽イオン、負(マイナス)の電気を帯びたものは陰イオンと呼びます。
ケイ素(Si)は他の原子と結びつく際に、4価の陽イオン(Si⁴⁺)として振る舞います。
これは、ケイ素原子が4つの電子(−)を放出して、プラス4の電荷を持っているという状態です。
一方で、酸素(O)は2価の陰イオン(O²⁻)としての性質を示します。
酸素原子は2つの電子(−)を受け取ることで、マイナス2の電荷を持ちます。
SiO₄四面体は1つのケイ素原子と4つの酸素原子の結合なので、
ケイ素(Si⁴⁺)の電荷:+4
酸素(O²⁻)の電荷:(-2) × 4 = (-8)
全体の電荷:+4 + (-8) = -4
四面体全体としてマイナス4の電荷を持つことになります。
ゆえに、ひとつひとつの四面体はケイ酸イオン(SiO₄⁴⁻)として扱われます。
4. 電気的な安定
電気のバランスという意味では、電荷が0の状態が安定していると言えるので、電気を帯びたイオンの状態は不安定です。
そのため、イオンは他のイオンと結合して電気的に中性(電荷0)になろうとします。
ケイ酸イオン(SiO₄⁴⁻)も当然、そのままでは不安定なので、
これを解消するために反対の電荷を持つイオンと結合します。
これが、先の「石英の成分」と「何か」が結合して「電気的に中和された」化合物
として ”塩(えん)” になる理由です。
では、この「何か」の正体は?というと、
金属イオン
です。
ケイ酸イオン(SiO₄⁴⁻)は4価の陰イオン(−4)なので、中和のために必要なイオンは、
同じく4価の電荷を持つ陽イオン(+4の金属イオン)です。
このとき、4価の金属イオンひとつと1対1で結合することもあれば、
1〜3価の金属イオンが複数集まって合計4価になる形で結合する場合もあります。
結合の組み合わせは、金属イオンの種類と相まってさまざまなパターンが存在するため、
ケイ酸塩鉱物の多様性を生み出す一因となっています。
※具体的な結合の様子は、次回解説します。
5. まとめ
少しまわりくどい説明をしましたが、まとめると次のようになります。
「ケイ酸塩(鉱物)」とは?
- ケイ酸イオン(SiO₄⁴⁻)と金属イオンが結合した塩(えん)である。
- その構造は、中心にケイ素原子があり、それを四つの酸素原子が取り囲むSiO₄四面体を形成している。
鉱物的な観点では、特に2つ目を重要視しているため、
『ケイ酸塩鉱物は、SiO₄四面体構造をもつ鉱物である』
と定義されることも多いです。
6. 終わりに
ケイ酸塩鉱物の本質を理解するのは、少し難易度が高いかもしれません。
それは、説明する側からしても同様で、
どうしても、内容が「化学の領域」に入ってしまうので、思ったより厄介です。
ズバリ、「〜である。」と言ってスマートに話をまとめると、化学の知識が前提の話になってしまうし、
一から説明しながら進めると、話が右往左往して本質がわかりづらくなってしまいます。
かといって、
表面をなぞっただけの説明だと、言ってることはわかるけどイメージがわかない、漠然とした話で終わってしまいます。
その辺のさじ加減が難しいところです。
ただの石好きの立場からすると、
『ケイ酸塩鉱物ってのは、石英の成分が基本で、それに色んなものが混ざってできたバリエーションでしょ。』
くらいで語るのがちょうどいいのですが。
さすがに、いろいろツッコミどころ満載になってしまうので、なるべく正確な解釈に基づいて説明したつもりです。
が、あくまで ”鉱物を知る” というのがテーマなので、化学的に誤解を生む表現があるかも知れませんがご了承ください。



